1.牛单B细胞技术原理
单个B细胞抗体制备技术是近年来新发展的一类快速制备单克隆抗体的技术,基于流式细胞分选技术进行单B细胞单抗制备,利用每个B细胞只含有一个功能性重链可变区DNA序列和一个轻链可变区DNA序列且只产生一种特异性抗体的特性,从动物的淋巴组织中收集B细胞,通过单克隆化技术从单个抗体分泌B细胞中扩增重链和轻链可变区基因,从而将收集到的B细胞扩增成单一来源的克隆群,然后选择抗体生产宿主,使其产生抗体[1] 。
牛单B细胞技术具体特异性强,批次间差异小等特点,由该方法制得的牛单克隆抗体是常用的单克隆抗体。目前,牛单B细胞技术制备的抗体在生物医学研究、诊断工具和治疗药物研发等方面有广泛应用[2]。

图1: 牛重组单克隆抗体制备(卡梅德生物科技(天津)有限公司 )
2. 牛单B细胞单抗制备流程
①动物免疫、PBMC分离。选择牛作为实验动物,并通过注射目标抗原(通常是目标蛋白或多肽)来激发免疫反应,免疫牛4-5次,以此激活牛的免疫系统,导致B细胞产生抗体。然后进行ELISA效价测定、免疫牛外周血采集和PBMC分离。
②流式分选。用PBMC流式分选方法来分选抗原特异性的单个B细胞。
③单B细胞培养筛选。将分选的单个B细胞先在体外进行5~20板96孔板单B细胞培养,然后将细胞培养的上清进行ELISA筛选或者FACS等前期介入检测。
④阳性克隆测序。挑选检测的至少20个阳性细胞克隆进行RT-PCR,来扩增其抗体可变区基因,然后进行测序。
⑤载体构建、抗体表达纯化。最后进行抗体的哺乳表达载体构建、细胞转染和ELISA验证。
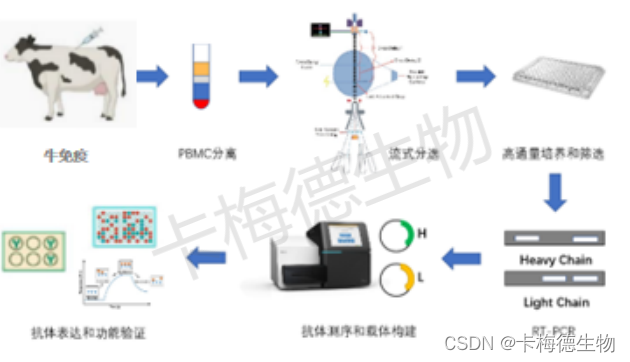
图2:牛单B细胞技术抗体制备流程图(卡梅德生物科技(天津)有限公司 )
3.单B细胞单抗制备优势
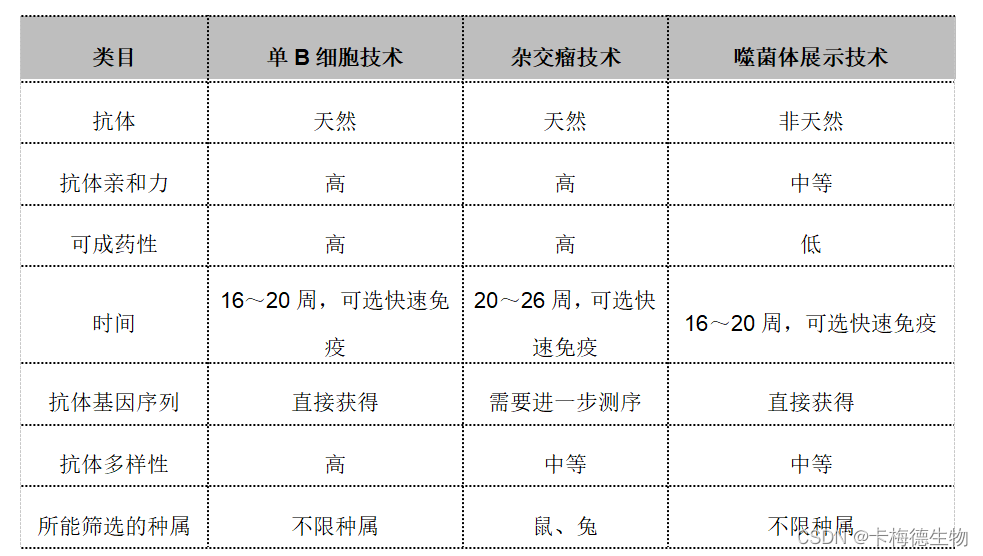
单B细胞技术能够根据B细胞的特性快速制备单克隆抗体,直接获取完整的单一来源抗体,该方法不限种属、效率高、特异性高、抗体亲和力高、可成药性高、基因多样性好且具有全天然源性,并且能够直接获得抗体基因序列[3] 。
4.牛单B细胞应用
牛单B细胞技术制备的抗体通常广泛应用于以下4个方面:
①药物研发。牛单B细胞技术制备的抗体能够被用于新药物的研发,尤其是在癌症治疗领域具有极大的应用前景。
②疫苗研制。牛单B细胞技术制备的抗体能够被用于提高疫苗的效力和特异性。
③免疫疗法。使用牛单B细胞技术制备的抗体可以用于免疫治疗,能够为消费者提供更加个性化的治疗。
④基础医学研究。抗体具有特异性和多样性,能够用于解析生物学过程和疾病机制。
5. 卡梅德生物能提供的服务及优势
卡梅德生物拥有丰富的经验积累、严格的质控体系,提供的单B细胞单抗制备服务的周期短、不限种属、可获得抗体序列,得到的抗体具有更高的特异性和亲和力。为了满足客户的不同需求,卡梅德生物能够提供从抗原设计,合成与修饰,到动物免疫,噬菌体文库构建与筛选,下游抗体修饰与应用鉴定等一站式技术服务。可咨询卡梅德生物官网获得详细信息。
参考文献
[1] Tan S H , Young D , Elsamanoudi S ,et al.Abstract 2565: Detection of ETV1 expression in human prostate tissue specimens using a novel and highly specific rabbit monoclonal antibody[C]//Proceedings: AACR Annual Meeting 2021; April 10-15, 2021 and May 17-21, 2021; Philadelphia, PA.2021.DOI:10.1158/1538-7445.AM2021-2565.
[2] Wallace J L , Arfors K E , Mcknight G W .A monoclonal antibody against the CD18 leukocyte adhesion molecule prevents indomethacin-induced gastric damage in the rabbit[J].Gastroenterology, 1991, 100(4):878-883.DOI:10.1016/0016-5085(91)90259-N.
[3] Powell, William C ,Hicks,et al.A new rabbit monoclonal antibody (4B5) for the immunohistochemical (IHC) determination of the HER2 status in breast cancer: comparison with CB11, fluorescence in situ hybridization (FISH), and interlaboratory reproducibility.[J].Appl Immunohistochem Mol Morphol, 2008, 15(5):510-1.DOI:10.1097/PAI.0b013e31802ced25.